Si vous êtes déjà inscrit, tapez juste votre adresse email puis votre mot de passe
Cas clinique de la semaine 17 - Embolie pulmonaire en MG en médecine générale
Introduction
Au cours de ce cas clinique, vous verrez :
- Quel score clinique utiliser en pratique clinique dans l'embolie pulmonaire ?
- Quand demander des D dimères et quand demander un scanner ?
- Quel anticoagulant choisir AOD vs AVK, quel AOD ?
- Quel bilan étiologique faire dans l'Embolie Pulmonaire en 2026 selon l'histoire clinique ?
Au terme de ce cas clinique, vous recevrez :
- Une fiche de synthèse des dernières recommandations à jour à appliquer
- Les points clefs à retenir sur l'embolie pulmonaire en 2026
- 100% Evidence Based Medicine, 100% MG, 100% pratique !
Cas clinique de la semaine 17 - Embolie pulmonaire en MG
Vous recevez en consultation Mme O, 48 ans pour une dyspnée d’apparition brutale lors du retour de voyage en voiture depuis la Bretagne. Elle présente un antécédent de tabagisme, un surpoids avec un IMC à 26 kg/m² et une péricardite virale. Elle n’a pas de douleur ni d’œdèmes au niveau des membres inférieurs. Ses constantes sont dans les limites de la normale, l'auscultation cardio pulmonaire est sans particularité.
Devant ce tableau clinique :
- Vous adressez la patiente aux urgences pour réalisation d’un TDM thoracique
- Vous adressez la patiente aux urgences pour dosage des d-dimères
- Vous évoquez une récidive de sa péricardite
- Son tableau clinique est rassurant, vous reconvoquez la patiente dans 48 heures
Les bonnes réponses sont B et C.
Réponse A : Faux. Adresser d'emblée pour TDM thoracique sans stratification du risque d'embolie pulmonaire expose à des faux positifs. Il faut retenir que si l'on suspecte une embolie pulmonaire (EP), avant tout examen complémentaire, il faut faire un score de probabilité clinique. Il y a beaucoup de scores disponibles dans le calcul de la probabilité clinique d'EP
Réponse B : Vrai. Si l'on calcule le score de Wells, la probabilité d'EP est faible ce sont donc les D-dimères qu'il est recommandé de demander. C'est la voie la plus sûre, la moins irradiante et la plus coût-efficace. Adresser aux urgences se justifie ici par l'apparition brutale et l'incertitude pré-test : la décision se joue en équipe avec biologie disponible 24h/24.
Réponse C : Vrai. Devant un ATCD de péricardite virale, la récidive reste un diagnostic différentiel plausible (récidive jusqu'à 30 % à 5 ans, European Society of Cardiology 2015). Mais évoquer la récidive ne dispense JAMAIS d'éliminer l'EP, pathologie potentiellement mortelle (mortalité EP non traitée ≈ 30 %). C'est l'application clinique du raisonnement bayésien : maintenir le diagnostic le plus grave plausible jusqu'à preuve du contraire.
Réponse D : Faux. Reconvoquer à 48 h sans bilan = perte de chance majeure. L'EP est « le grand simulateur » : 30 % des décès surviennent dans les 48 premières heures (PIOPED II). Constantes normales et absence de signes de TVP n'ont aucune valeur d'exclusion (Stein et al. NEJM 2006 : 50 % des EP confirmées ont une SpO₂ ≥ 95 %). La règle pédiatrique-adulte vaut : « pas vu = pas pris ».
L'essentiel à retenir en une slide :

🧠 Soft skill 👉🏻 Penser à voix haute & assumer l'incertitude ! Verbalisez devant la patiente votre raisonnement : « Vos symptômes peuvent venir d'une péricardite, mais je ne peux pas exclure une embolie pulmonaire ici, en cabinet. » Cette transparence transforme l'incertitude en décision partagée et justifie l'orientation aux urgences sans dramatiser. Le médecin qui sait dire « je ne sais pas, donc on sécurise » construit plus de confiance qu'un faux apaisement.
Dr Pauline Fra, pneumologue au CHU de Saint Etienne, commente le QCM :
Le dosage des d-dimères s’est avéré positif et l’angioscanner thoracique a confirmé le diagnostic d’embolie pulmonaire sous segmentaire gauche, de risque faible. Elle est rentrée à domicile, avec une prescription d’APIXABAN. Vous la revoyez en consultation 2 mois après.
Concernant la gestion des AOD :
- Au niveau biologique, la prescription d’APIXABAN allonge le TCA
- Il est contre-indiqué en cas de DFG inférieur à 15 ml/min/m² selon la formule de Cockcroft et Gault
- Il présente un risque de saignements moindre que le RIVAROXABAN
- Un dosage sanguin de l’APIXABAN est recommandé au cours du suivi
Les bonnes réponses sont A, B et C.
Réponse A : Vrai. L'apixaban est un inhibiteur direct et sélectif du facteur Xa. Il agit sur la voie commune de la cascade et allonge donc TP et TCA de façon variable, mais imprévisible et non corrélée à l'effet anticoagulant. Ces tests ne permettent ni le suivi ni l'ajustement (RCP HAS, Recommandations GIHP 2024). Si un dosage est nécessaire, seul le dosage spécifique anti-Xa apixaban est interprétable, dans des laboratoires calibrés.
Réponse B : Vrai. Apixaban est contre-indiqué si DFG < 15 mL/min/1,73 m². Adaptation entre 15 et 29 mL/min : 2,5 mg × 2/j. Réduction également si 2 critères parmi : âge ≥ 80 ans, poids ≤ 60 kg, créatininémie ≥ 133 µmol/L (étude ARISTOTLE). Le DFG doit être réévalué tous les 6 à 12 mois, voire trimestriellement chez la personne âgée fragile, car l'insuffisance rénale aiguë est la 1ʳᵉ cause d'accident hémorragique sous AOD !
Réponse C : Vrai. Apixaban diminue d'environ 54 % le risque hémorragique majeur vs rivaroxaban, principalement digestif. Mécanismes : demi-vie plus courte (12 h vs 12 h aussi mais Cmax plus basse), schéma 2 prises/j (vs 1 pour rivaroxaban) lissant le pic plasmatique. Aucun essai randomisé head-to-head ne l'a confirmé : niveau de preuve = études observationnelles (LOE B-NR).
Réponse D : Faux. ANSM/HAS/GIHP 2024 : pas de monitoring biologique en routine pour les AOD. Le dosage spécifique n'est indiqué que dans 4 situations : hémorragie active grave, geste invasif urgent, suspicion de surdosage/sous-dosage, suspicion d'inobservance. Demander un dosage en suivi banalisé crée plus de problèmes (faux positifs, anxiété, sur-prescription) qu'il n'en résout.
L'essentiel à retenir en une slide :

🧠 Soft skill 👉🏻 Décision partagée. Annoncez à Mme O le pourquoi de chaque question avant de la poser : « Je vais reprendre votre traitement, vérifier votre fonction rénale et discuter du risque saignement. » Co-construire la balance bénéfice/risque AOD est ce qui transforme une ordonnance subie en traitement adhéré. L'observance des AOD chute à 50 % à 1 an dans les études en vie réelle (Banerjee, BMJ 2020) — la conversation vaut le dosage biologique 😉
Dr Pauline Fra, pneumologue au CHU de Saint Etienne, commente le QCM :
Dans le cadre du bilan étiologique de cette embolie pulmonaire, vous prescrivez à Mme O :
- Un échodoppler veineux des membres inférieurs
- Un dépistage gynécologique avec consultation spécialisée
- Une recherche de Syndrome des Anticorps anti Phospho Lipides (SAPL) en 1ère intention
- Une recherche de la mutation du facteur II et du facteur V Leiden en 1ère intention
Toutes les réponses sont bonnes.
Réponse A : Vrai. 30 à 50 % des EP s'accompagnent d'une TVP des membres inférieurs, souvent asymptomatique (Kearon, Chest 2016). L'écho-doppler veineux des MI a deux intérêts : confirmer une source emboligène persistante (impacte la durée d'anticoagulation) et fournir un comparatif pour le diagnostic ultérieur de récidive vs séquelles. Examen non irradiant, peu coûteux, opérateur-dépendant : à demander à un radiologue ou angiologue formé.
Réponse B : Vrai. EP « non provoquée » chez femme < 50 ans : la recherche d'un cancer occulte est recommandée (ESC 2019, INCa). Bilan minimal validé : examen clinique complet + dépistages adaptés à l'âge et au sexe (mammographie, frottis cervical, recherche de sang dans les selles si > 50 ans), interrogatoire gynécologique (saignements, ménopause, THM, contraception œstroprogestative). L'étude SOME (NEJM 2015) a montré qu'un bilan extensif (TDM TAP) n'apporte aucun bénéfice par rapport au dépistage limité.
Réponse C : Vrai. Le SAPL est la 1ʳᵉ thrombophilie acquise à rechercher chez la femme jeune avec EP non provoquée.
Critères de Sydney révisés (Miyakis 2006) :
- Anticorps anti-cardiolipine IgG/IgM,
- Anti-β2-glycoprotéine 1,
- Anticoagulant lupique à confirmer par un 2ᵉ dosage à 12 semaines d'intervalle.
🚨 Conséquence majeure : un SAPL triple-positif contre-indique les AOD (étude TRAPS, Pengo Blood 2018) et impose les AVK au long cours. C'est une des rares indications (avec la valve mécanique) des AVK versus les AOD en 2026.
Réponse D : Vrai. Recherche de thrombophilie héréditaire (Facteur V Leiden, mutation prothrombine G20210A, déficit en AT/PC/PS) chez patient < 50 ans avec EP non provoquée ou ATCD familiaux thromboemboliques.
🚨 Piège : sous AOD, l'anticoagulant lupique est faussement positif par interférence avec les tests phospholipides-dépendants. Une fenêtre thérapeutique de 5 jours (relais HBPM 24-48 h avant prélèvement) est requise !
L'essentiel à retenir en une slide :

🧠 Soft skill => Repérer les indices et l'agenda caché du patient. « Avez-vous d'autres symptômes ? » est rarement suffisant. Cherchez activement les signes faibles : amaigrissement, modification du transit, saignements gynécologiques, ATCD familiaux peu détaillés à la 1ʳᵉ consultation. Une EP non provoquée à 48 ans est aussi une opportunité de rattrapage des dépistages oubliés. La consultation post-événement est un moment où la patiente est receptive => "capitalisez sur l'inquiétude" pour transformer l'inquiétude en action préventive utile.
Quel bilan demander en pratique de MG du point de vue étiologique ? Jusqu'où pousser la complexité du bilan => Chez qui demander un bilan de thrombophilie par exemple ?
Vous revoyez votre patiente 1 mois après, avec les résultats du bilan de thrombophilie que vous lui avez prescrit. Celui-ci met en évidence un SAPL. Vous décidez de relayer son traitement anticoagulant par AVK.
- Vous introduisez d’emblée un traitement par COUMADINE 6 mg sous couverture par APIXABAN
- Vous faites un dosage de l’INR tous les jours jusqu’à obtenir 2 INR dans la cible, une fois la COUMADINE introduite
- Vous arrêtez l’APIXABAN uniquement 24 heures après obtention de l’INR dans la cible
- Si le 1er INR dosé à 72h est < 1.3, vous majorez la COUMADINE de 2 mg
Toutes les réponses sont bonnes.
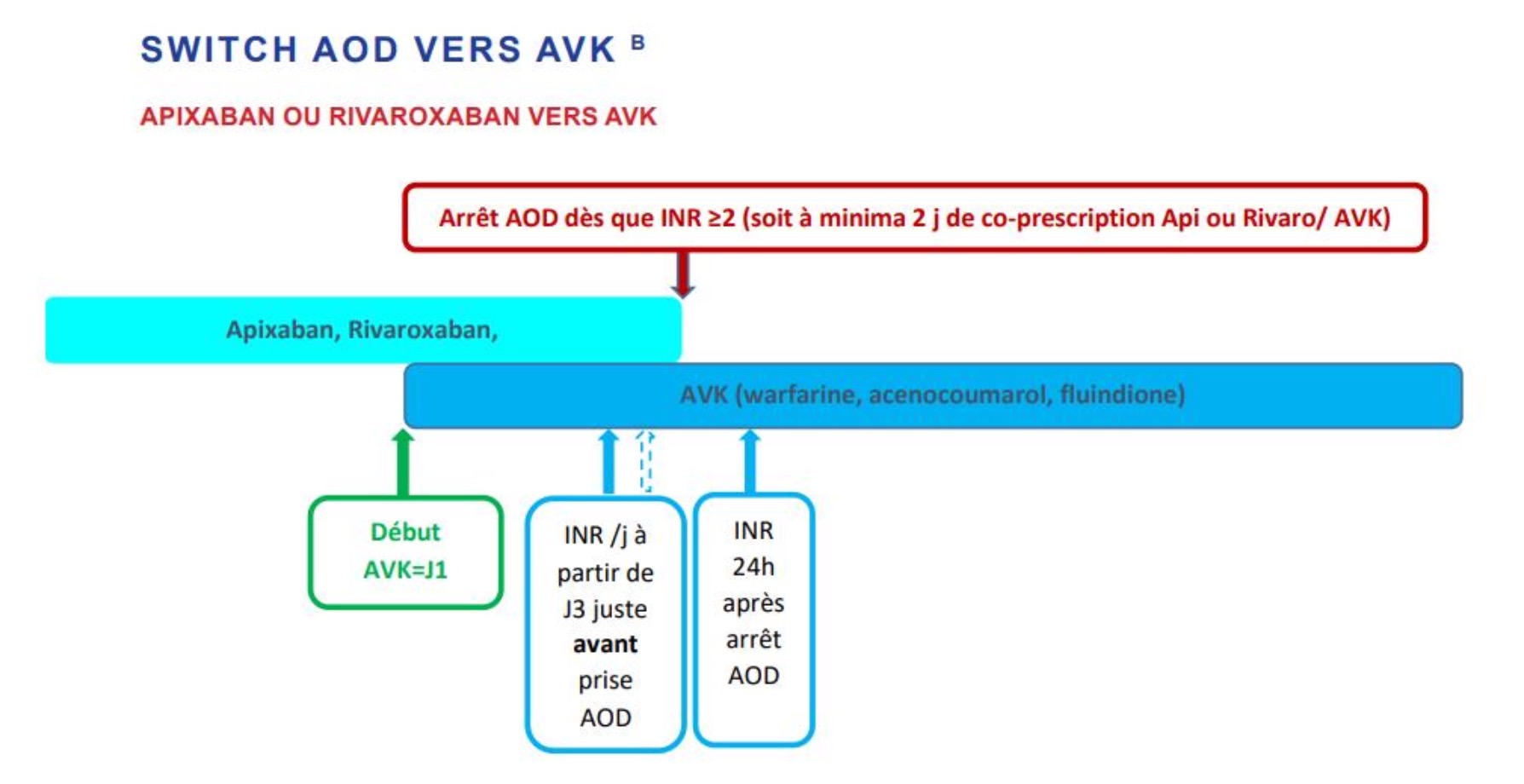
Réponse A : Vrai. Schéma HAS/SFAR : introduction COUMADINE® (warfarine) à dose d'attaque (5-6 mg/j chez l'adulte non fragile) sous couverture poursuivie de l'AOD, sans chevauchement à éviter (contrairement au relais HBPM). C'est le « bridging par AOD » : on continue l'apixaban jusqu'à ce que l'INR soit en cible 2 fois consécutives. La COUMADINE atteint son efficacité après 5 à 7 jours (demi-vie facteur II ≥ 60 h).
Réponse B : Vrai. À partir de J3, dosage INR quotidien toujours avant la prise d'AOD du matin pour limiter l'interférence in vitro. Critère d'arrêt de l'AOD : 2 INR consécutifs en cible. Cet algorithme est l'application directe du schéma GIHP/HAS 2024 du switch AOD → AVK, dont la sécurité a été validée a posteriori dans le registre français FRENCHIE (sans excès thrombotique ni hémorragique).
Réponse C : Vrai. Arrêt de l'apixaban 24 h après le 2ᵉ INR en cible. Dans le SAPL avec triple positivité ou thrombose artérielle, cible INR 3-4 (recommandations EULAR 2019, BSH 2020). Dans le SAPL « simple » avec thrombose veineuse seule, cible INR 2-3 acceptable. La temporalité du switch est critique : un arrêt prématuré expose à la récidive thrombotique, un arrêt trop tardif au surdosage.
Réponse D : Vrai. Algorithme classique d'adaptation posologique de la warfarine (référentiel SFAR, GIHP) : si INR à 72 h < 1,3 → +2 mg ; entre 1,3 et 1,5 → +1 mg ; entre 1,5 et 1,7 → +0,5 mg. Au-delà, on stabilise et on espace les contrôles. La pharmacogénétique (CYP2C9, VKORC1) explique 40 % de la variabilité individuelle, mais le génotypage n'est pas recommandé en routine.
L'essentiel à retenir en une slide :

🧠 Soft skill => Écoute active. Le passage d'un AOD (1 prise, pas de contrôle) aux AVK (alimentation, INR hebdo, interactions) est vécu comme une régression. Reconnaissez l'émotion : « Je comprends que ce changement vous inquiète, voici pourquoi il est important pour votre type de pathologie. » Donnez un filet de sécurité écrit : seuils d'alerte hémorragiques (gencives, urines, hématomes), conduite à tenir en cas de surdosage, numéro à appeler. Le carnet AVK rempli à chaque consultation reste un outil de pacte thérapeutique.
Votre patiente revient vous voir 1 an après car elle doit subir une cholécystectomie dans 1 mois. Elle a présenté une thrombose artérielle digestive sans signe de gravité il y a 4 mois. A ce propos, elle s’interroge concernant son traitement anticoagulant.
- Vous prévoyez un relai par AOD afin d’encadrer le geste chirurgical et diminuer le risque de saignement post-opératoire
- Vous prévoyez un relai par HBPM pour encadrer le gente, en interrompant les AVK 5 jours avant l’intervention
- Vous prévoyez un saut de prise des AVK à J-2, si l’INR est bien contrôlé
- Aucune réponse exacte
La bonne réponse est B.
Réponse A : Faux. Aucun relai AVK → AOD chez ce profil. Le SAPL avec antécédent thrombotique veineux ET artériel est une contre-indication formelle aux AOD (étude TRAPS interrompue précocement pour excès d'événements thrombotiques sous rivaroxaban ; recommandations EULAR 2019, ISTH 2020). Le « confort » d'un AOD ne justifie jamais une perte d'efficacité chez un patient à très haut risque thrombotique.
Réponse B : Vrai. Schéma Société Française d'Anesthésie et de Réanimation « gestion péri-opératoire des AVK chez patient à haut risque thrombotique » : arrêt warfarine J-5, contrôle INR à J-1 (cible < 1,5 pour intervention), relais HBPM curative à dose adaptée au poids dès INR < 2 (typiquement J-3), dernière injection HBPM 24 h avant chirurgie. Reprise post-opératoire : HBPM dose préventive à H6-H8, curative à H24-H48 selon hémostase, AVK reprise dès H24, arrêt HBPM quand INR ≥ 2 sur 2 dosages.
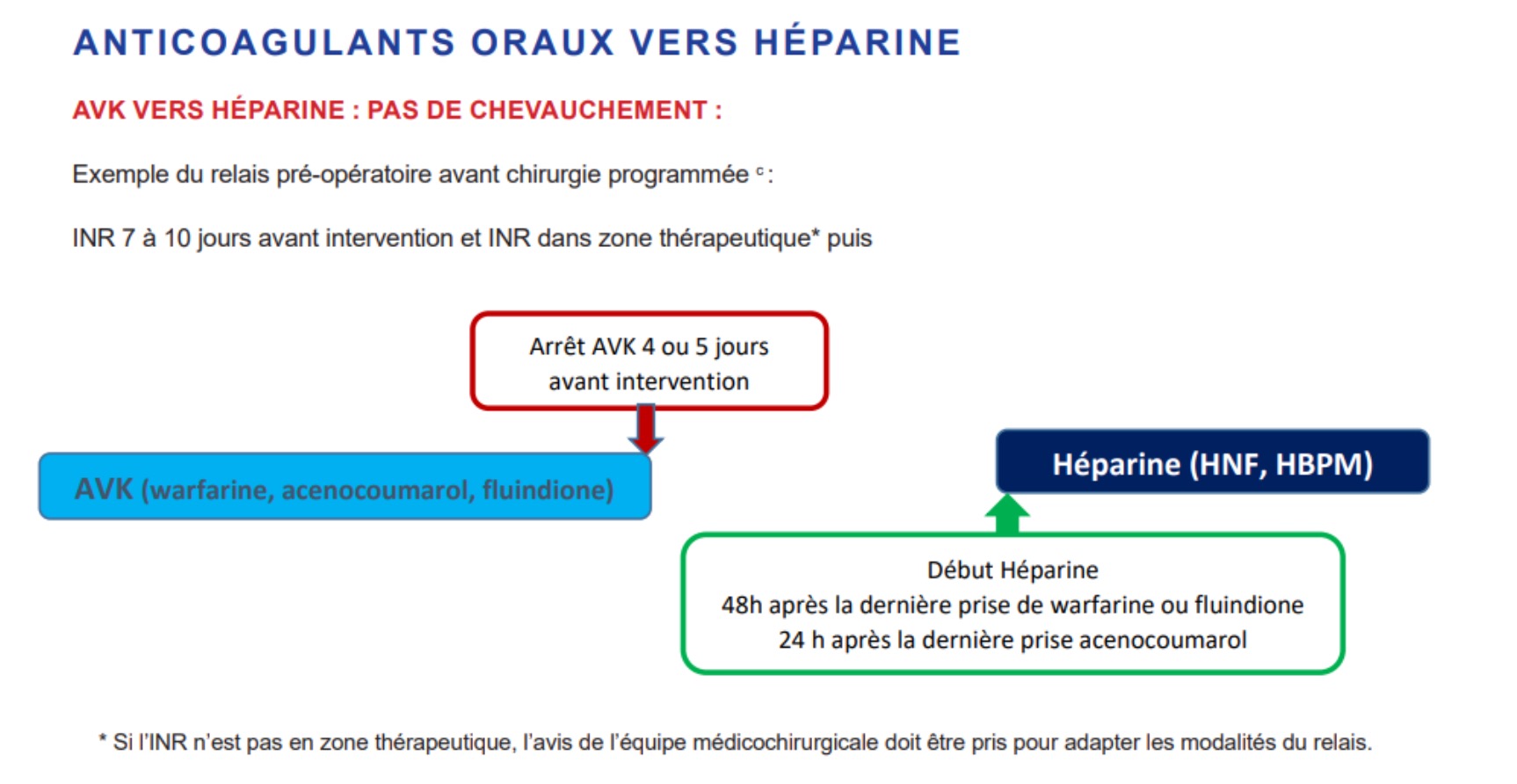
Réponse C : Faux. Saut de prise à J-2 = stratégie acceptable uniquement chez patient à bas risque thrombotique (FA non valvulaire CHA₂DS₂-VASc faible). Inapplicable ici : la demi-vie du facteur II (60-72 h) ne permet pas une décroissance suffisante de l'INR en 48 h, et surtout l'absence de bridging laisse une fenêtre thrombotique de plusieurs jours inacceptable chez un SAPL. C'est l'erreur typique du « simple = sûr » qui oublie le risque thrombotique sous-jacent.
L'essentiel en une slide :

🧠 Soft skill => Cadrer, résumer, savoir escalader. Le préopératoire d'un patient anticoagulé complexe ne se gère pas seul. Rédigez un résumé structuré (1 page : ATCD, indication anticoagulation, cible INR, calendrier précis) à transmettre au chirurgien et à l'anesthésiste. Validez le plan en RCP médico-chirurgicale si triple positivité ou geste à fort risque hémorragique. La capacité à dire « je passe la main pour cette décision » et à coordonner les acteurs est capital pour le MG "pivot" des soins.
Messages clés à retenir
Fiche de synthèse sur l'embolie pulmonaire :

Les points clefs à retenir :
1) Utiliser les scores de probabilités cliniques avant de penser aux examens complémentaires, en MG : score de WELLS
2) Faible proba <4 => D dimères Forte proba >4 => TDM thoracique
3) Le traitement de référence est les AOD, la durée dépend de la cause : EP provoquée versus EP non provoquée (pas de consensus dans ce cas demander avis spé)
4) Privilégier l'Eliquis permet de réduire le risque hémorragique : Etude COBBRA du NEJM d'Avril 2026
5) Qui dit AOD dit surveillance du DFG !
6) Dans le bilan étiologique, d'une EP non provoquée : pensez à la triade = Thrombophilie / SAPL et Cancer occulte
7) Le switch AOD => AVK se fait avec un chevauchement jusqu'à obtenir l'INR dans la cible
8) Le switch AOD => Héparine => Pas de chevauchement.


